【プレスリリース】遺伝子発現と脂質変換を連動させた人工細胞 ― 刺激応答型の動的膜非対称性を実現 ―
プレスリリース資料はこちら
本学の神谷厚輝准教授、李水民(当時 博士前期課程 学生)、馬塲康太朗(博士後期課程2年)は、リン脂質組成対称膜リポソームから外部刺激によるスイッチングによって発現した酵素によってリン脂質非対称膜リポソームへと動的に変化させ、膜タンパク質の機能の活性化に成功しました。この成果は、2026年4月27日付の国際学術誌Communications Biologyに掲載されました。
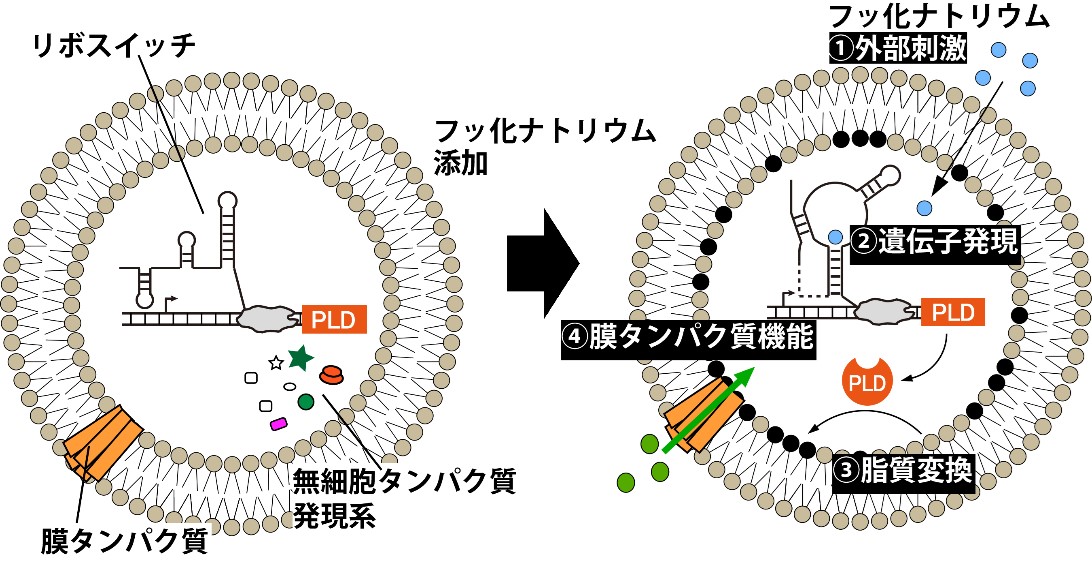
細胞では、膜の内側と外側でリン脂質の種類が異なる「リン脂質非対称膜構造」が、物質輸送やシグナル伝達などの重要な機能を担っています。この構造を人工的に再現したリン脂質非対称膜リポソームの作製はありますが、外部刺激で動的に膜構造を変換する技術はほとんどありませんでした。本研究では、化学物質(フッ化物)に応答して遺伝子発現を制御する「リボスイッチ」を利用し、人工細胞膜のリポソーム内で酵素を合成しました。その酵素反応によってリン脂質の種類を変換し、膜の内側だけに特定のリン脂質を生成することで、機能的な膜の非対称性を自律的に作り出すことに成功しました。さらに、この膜の変化により、膜タンパク質(ナノポア)が活性化され、分子の出入りが制御されることも実証しました。つまり、外部刺激 → 遺伝子発現 → 脂質変換 → 膜タンパク質機能の発現という一連の流れをリポソーム内で実現しました。本技術は、環境に応答して機能を変える“外部刺激応答型人工細胞”の基盤となるものであり、将来的には、薬剤をその場で合成・放出する次世代ドラッグデリバリーや、生命現象の解明、人工細胞間でコミュニケーションして機能化する人工細胞組織の創製への応用が期待されます。
1.本件のポイント
- 外部刺激で“膜の非対称性”を動的に生成する仕組みの構築
リボスイッチによる遺伝子発現制御と酵素反応(ホスホリパーゼD)を組み合わせることで、人工細胞内でリン脂質組成を変換し、内外で異なるリン脂質膜構造(非対称性)を動的に形成することに成功。 - 膜構造の変化を利用した“機能発現の制御”の実証
生成された負電荷脂質非対称膜により、膜タンパク質(MscL)が活性化され、分子輸送に成功。膜の状態変化がそのまま機能発現につながることを示した。
2.本件の概要
国内外で、人工細胞膜であるリポソーム(注1)内にさまざまな生体分子を封入したボトムアップ型人工細胞の研究が盛んに行われており、生命機能の再構築や医療応用に向けた展開が期待されています。近年では、細胞のように外部刺激に応答してリポソーム内で機能を発現する人工細胞の開発も進んでいます。本研究では、化学物質(フッ化物)に応答して遺伝子発現を制御する「リボスイッチ」を利用し、リポソーム内部で酵素(ホスホリパーゼD:PLD)を発現させ、PLDにてリン脂質分子が変換されることでリン脂質組成非対称膜リポソームへの動的な変換が起こる人工細胞の開発に成功しました。リポソーム内には、リボスイッチを搭載したPLD遺伝子プラスミドと無細胞タンパク質発現系を封入しています。リポソーム外液にフッ化ナトリウムを添加すると、これが膜を透過して内部に流入し、リボスイッチが活性化されてPLDが発現します。発現したPLDは、リポソーム膜内側のホスファチジルコリン(PC)を、負電荷を持つホスファチジル酸(PA)へと変換します。その結果、膜の内外で脂質組成が異なる非対称膜構造(外膜:PC、内膜:PC+PA)を動的に形成することに成功しました。この非対称膜はフッ化ナトリウム添加後約20分から形成されはじめ、一定時間後には約10〜20 mol%のリン脂質がPAへと変換されました(図1)。さらに、リポソーム膜にコレステロールを添加すると膜流動性が低下し、形成された非対称膜構造がより安定に維持されることが分かりました。また、負電荷脂質によって開孔する膜タンパク質である機械感受性チャネルMscLをリポソームに再構成したところ、フッ化ナトリウム添加後1時間でカルセインの輸送が顕著に観察されました(図2)。これは、PLDによるPA生成によってMscLが活性化され、分子輸送機能が誘導されたことを示しています。本研究では、外部刺激 → 遺伝子発現 → 脂質組成変換 → 膜タンパク質機能の発現という一連のプロセスを人工細胞内で実現しました。外部刺激によって膜構造を動的に変換し、非対称膜を形成する技術は本研究が初めてです。本技術は、環境に応答して機能を変化させる「外部刺激応答型人工細胞」の基盤となるものであり、将来的には、薬剤のその場合成・放出を可能にする次世代ドラッグデリバリーや、生命現象の解明、さらには人工細胞同士が相互作用して機能する人工細胞組織の創製への応用が期待されます。
本成果は、2026年4月27日付で学術誌「Communications Biology」に掲載されました。
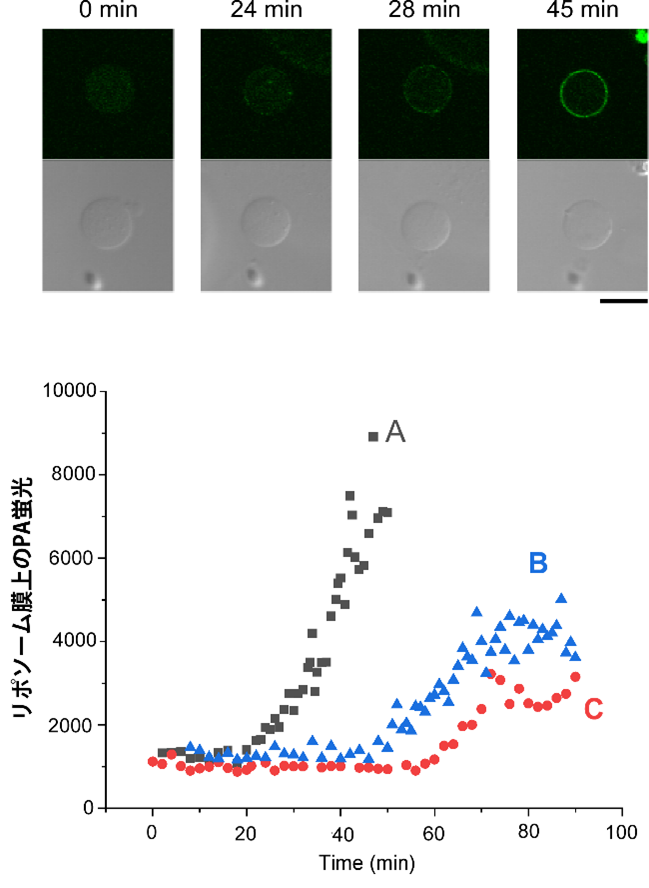
図1 フッ化ナトリウム添加後のPLDによるリポソーム膜の脂質変換。PLDによってPCからPAに変換されると、PAに特異的に結合する蛍光分子が結合し可視化されました。
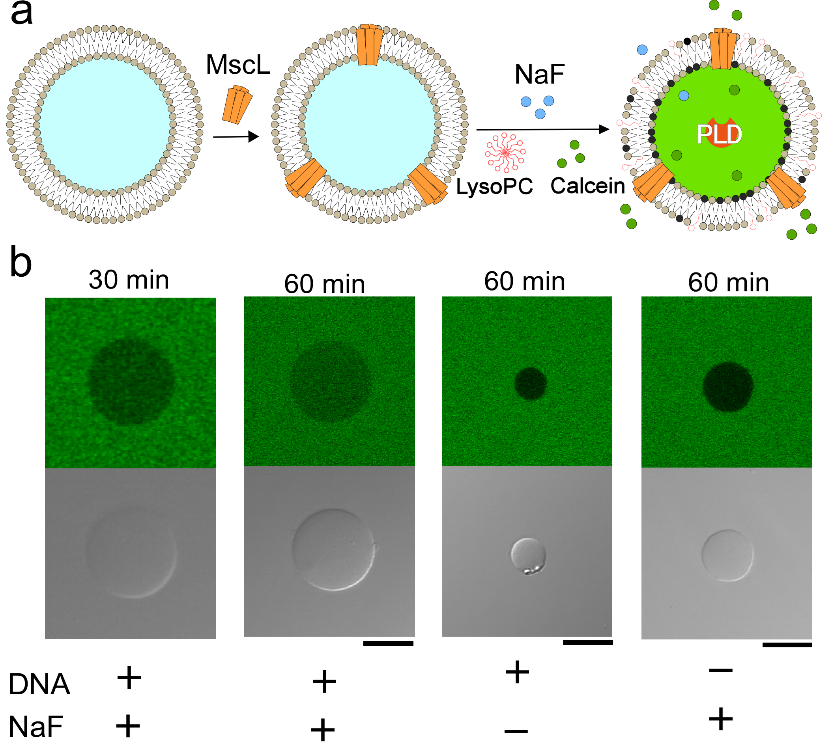
図2 外部刺激によってリポソーム内のPCをPAへの変換による機械感受性チャネルMscLの機能の活性化。DNAあり、NaF(フッ化ナトリウム)ありの場合、カルセインのリポソーム内の流入が観察されました。
用語
(注1) リポソーム: 細胞膜と同じリン脂質二重膜から構成された人工小胞。生体分子を再構成して生命機能の理解やドラッグデリバリーシステムの担体に使われている。
3.発表雑誌
雑誌名: Communications Biology
論文題名: Riboswitch-controlled lipid conversion enables functional membrane asymmetry in artificial cells
著者: Koki Kamiya(責任著者), Sumin Lee, Kotaro Baba
DOI番号 : https://doi.org/10.1038/s42003-026-09890-7
4.発表者情報
群馬大学 大学院理工学府 物質・環境部門 応用化学プログラム
神谷厚輝 准教授
李水民(当時 博士前期課程学生)
馬塲 康太朗(博士後期課程2年)
5.謝辞
本研究は、日本学術振興会(JSPS) 科研費 基盤研究(B) JP22H01874、学術変革領域研究(B)JP24H00889からの支援を受けて行われました。
6.本件に関するお問い合わせ先
<研究に関すること>
群馬大学大学院 理工学府 物質・環境部門 応用化学プログラム 生命分子機能化学研究室
准教授 神谷 厚輝 (かみや こうき)
Tel:0277-30-1342
E-mail:kamiya@gunma-u.ac.jp
神谷研究室のホームページ:http://kamiya.chem-bio.st.gunma-u.ac.jp/index.html
<報道に関すること>
群馬大学桐生地区事務部庶務係(広報担当)
Tel: 0277-30-1014 Fax: 0277-30-1020
E-mail:rikou-pr@ml.gunma-u.ac.jp
